Nội dung bài viết
Hợp chất vô cơ là những hợp chất hóa học thông dụng, có tính ứng dụng cao trong đời sống. Vậy hợp chất vô cơ là gì, nó được định nghĩa và phân loại như thế nào? Hãy cùng Vietchem tìm hiểu về đặc điểm nhận dạng cũng như tính chất và ứng dụng của chúng.
1. Hợp chất vô cơ là gì?
Đây là tên chung cho các hợp chất hóa học không có nguyên tử cacbon trong cấu trúc, ngoại trừ các trường hợp ngoại lệ sau:
- khí CO2
- khí CO2
- H2CO3
- muối cacbonat
- Hiđrocacbonat
- cacbua kim loại
Ảnh 1: Đây là những hợp chất không có cacbon trong thành phần
Các hợp chất vô cơ được coi là kết quả tổng hợp của nhiều quá trình địa chất. Chúng tồn tại rất nhiều trong tự nhiên và còn được con người tổng hợp trong phòng thí nghiệm, nhà máy, khu nghiên cứu và cả trong sinh hoạt hàng ngày.
2. Có mấy loại hợp chất vô cơ?
Dưới đây là các nhóm hợp chất vô cơ chính và phổ biến nhất:
2.1. Oxit
Một hợp chất được tạo thành từ hai loại nguyên tố hóa học khác nhau, bao gồm một nguyên tố oxy và nguyên tố còn lại không phải flo.
- Công thức chung của oxit: MxOy trong đó M là nguyên tố không phải O, x và y là chỉ số và đại lượng của các nguyên tố.
- Ví dụ: Fe2O3; CuO, Na2O, BaO
2.2. Axit
Đây là những hợp chất hòa tan trong nước, có công thức chung HxA. Trong đó A là bazơ axit và x là hóa trị của chất đó.
Ví dụ: H2SO4, HCl, HBr, HNO3…
2.3. Căn cứ
Đây là những hợp chất vô cơ có khả năng phân ly trong dung dịch nước, từ đó tạo ra ion OH- có công thức chung M(OH)n. Trong đó M là kim loại, n là hóa trị của kim loại đó.
Ví dụ: NaOH, Ba(OH)2, KOH, Ca(OH)2

Ảnh 2: NaOH là bazơ chung
2.4. Muối
Đây là những hợp chất hóa học được tạo thành từ kim loại (cation) và gốc axit (anion).
Ví dụ: KMnO4, NaCl, Na3PO4, CaCO3.
3. Các hợp chất vô cơ thông dụng
Nhưng phải nói rằng, hợp chất vô cơ rất phổ biến và phổ biến trong mọi lĩnh vực của đời sống. Dưới đây là những hợp chất vô cơ phổ biến nhất và có tính ứng dụng cao.
- Axit điển hình: H2SO4; HCl; HNO3; HF; H3PO4; H2CO3;
- Một số bazơ thông dụng: NaOH, Ca(OH)2, Ba(OH)2, KOH, Al(OH)3;
- Các muối thông dụng: NaCl, CuSO4; NaHCO3; NaNO3; FeCl2; AgNO3; FeSO4
4. Kể tên các hợp chất vô cơ
Trừ một số trường hợp đặc biệt, các hợp chất vô cơ đều có công thức chung. Cùng xem hướng dẫn đọc tên các hợp chất vô cơ của Vietchem:
4.1. Gọi tên oxit
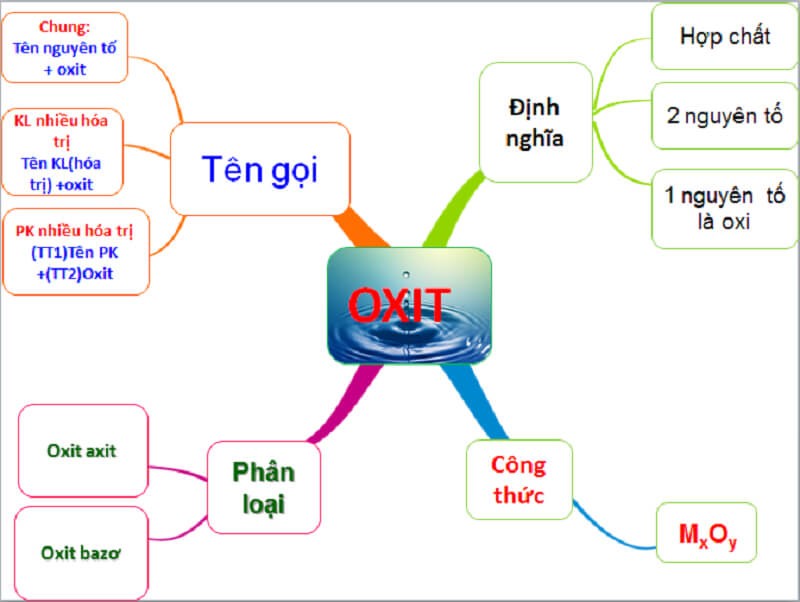
Ảnh 3: Cách gọi tên oxit theo thành phần
Trường hợp oxit oxi với kim loại:
Tên kim loại (có hóa trị của kim loại nếu là kim loại có hóa trị lớn hơn 1) + tên oxit.
Trường hợp oxit là hỗn hợp của oxy và phi kim, đặt tên theo cách sau:
Tiền tố chỉ số nguyên tử của phi kim đó + tên phi kim + tiền tố chỉ số nguyên tử oxy trong công thức + oxit
4.2. Cách đặt tên căn cứ
Tên kim loại (kèm số hóa trị nếu hóa trị lớn hơn 1) + Hydroxide
4.3. Cách gọi tên axit
- Với axit không chứa oxit: Axit + tên phi kim + hydric
- Axit giàu oxi: Tên axit + phi kim trong axit + ic
- Axit có ít nguyên tử oxi: Axit + tên phi kim + hưng phấn
4.4. Cách đọc tên muối
Tên kim loại (kèm theo số hóa trị) + tên bazơ axit
5. Sơ đồ tư duy về hợp chất vô cơ
Bản đồ tư duy sử dụng hình ảnh để thể hiện kiến thức tổng quát về mối quan hệ giữa các hợp chất vô cơ với nhau. Đặc biệt, nó còn giúp người xem hiểu được cách phân loại cơ bản của các hợp chất vô cơ.
Dưới đây là những mẫu sơ đồ tư duy ghép phổ biến và độc đáo nhất mà bạn đọc, học sinh có thể tham khảo:
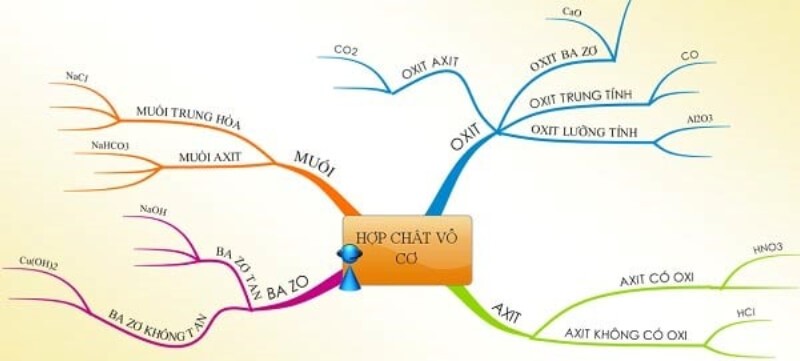
Ảnh 4: Sơ đồ tư duy số 1 về hợp chất vô cơ
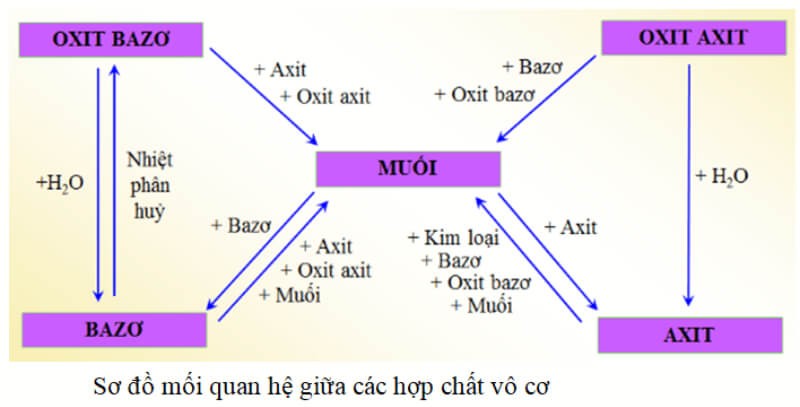
Ảnh 5: Sơ đồ tư duy số 2 về hợp chất vô cơ
6. Một số bài tập về hợp chất vô cơ
Bài học 1: Đề bài: Hoàn thành chuỗi phản ứng sau: Na – Na2O – NaOH – Na2CO3 – NaCl NaOH – NaHCO3
Giải pháp:
- 4Na + O2 → 2Na2O (điều kiện nhiệt độ)
- Na2O + H2O → 2NaOH
- 2NaOH + CO2 → Na2CO3 + H2O
- 2HCL + Na2CO3 → 2NaCl + CO2 + H2O
- 2NaCl + H2O → 2NaOH + Cl2 + H2
- NaOH + CO2 → NaHCO3
Bài học 2: Có 3 chất rắn màu trắng đựng trong các chai riêng biệt, không có nhãn mác, tên gọi. Đó là NaCl, Na2CO3 và 1 chai hỗn hợp Na2CO3 + NaCl. Xác định các chất có trong mỗi lọ trên bằng phương pháp hóa học. Chứng minh cách tiến hành, viết các phương trình hóa học xảy ra trong quá trình đó.
Giải pháp:
Trong mỗi lọ lấy một ít hỗn hợp cho vào ống nghiệm, nhớ đánh số để nhận biết.
- Sau đó nhỏ dung dịch Ba(NO3)2 vào từng ống nghiệm. 2 ống xuất hiện kết tủa là ống hỗn hợp hoặc ống chứa Na2CO3. Ống không có hiện tượng gì có thể nhận biết là NaCl. Nguyên nhân là do Na2CO3 phản ứng với Ba(NO3)2 tạo thành muối Ba kết tủa.
- Tiếp tục nhỏ giọt AgNO3 vào hai ống trên. Ống kết tủa tiếp theo là ống chứa hỗn hợp, ống còn lại chứa Na2CO3. Vì NaCl phản ứng với AgNO3 còn Na2CO3 thì không.
Các phương trình phản ứng xảy ra trong quá trình này là:
- Na2CO3 + Ba(NO3)2 → BaCO3 (kết tủa) + 2NaNO3
- AgNO3 + NaCl → AgCl (kết tủa) + NaNO3
Như vậy, Vietchem đã cung cấp cho bạn những thông tin cơ bản để bạn có cái nhìn tổng quan về các hợp chất vô cơ. Để mua và tìm hiểu về ứng dụng hóa chất hãy liên hệ ngay với Vietchem để cập nhật thông tin nhanh nhất.


Nội dung được phát triển bởi đội ngũ Meraki Center với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@merakicenter.edu.vn