Al + S → Al2S3 – Hướng dẫn cân bằng phản ứng hóa học của tất cả phương trình hóa học thường gặp giúp bạn học tốt môn Hóa.-Al + S → Al2S3
Al + S → Al2S3
Phản ứng Al + S tạo ra Al2S3 thuộc loại phản ứng oxi hóa khử, phản ứng hóa hợp đã được cân bằng chính xác và chi tiết nhất.
Bên cạnh đó là một số bài tập có liên quan về Al có lời giải, mời các bạn đón xem:
2Al + 3S → Al2S3
Điều kiện phản ứng
– Nhiệt độ cao (150 – 2000C)
Cách thực hiện phản ứng
– Cho Al tác dụng với S.
Hiện tượng nhận biết phản ứng
Al màu trắng bạc tác dung với S màu vàng tạo muối màu trắng Al2S3.
Bạn có biết
Tương tự Al, các kim loại khác (trừ Pt, Au) có phản ứng với S tạo muối sunfua
Ví dụ 1:Phương trình phản ứng nào sau đây đúng?
A. Na + S 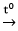 NaS2
NaS2
B. Cu + 2S → Cu2S
C. 4K + O2 → 2K2O
D. 2Al + 3S 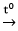 Al2S3
Al2S3
Hướng dẫn giải
Chọn D.
A. 2Na + S 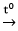 Na2S
Na2S
B. 2Cu + S 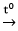 Cu2S
Cu2S
C. 4K + O2 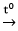 2K2O
2K2O
Ví dụ 2:Tính khối lượng Al tác dụng vừa đủ với 3,2 gam S để tạo thành muối Al2S3?
A. 0,9 gam. B. 1,8 gam. C. 2,7 gam. D. 4,5 gam.
Hướng dẫn giải
Chọn B.
2Al + 3S 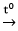 Al2S3
Al2S3
nS=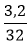 =0,1 mol ⇒ nAl=
=0,1 mol ⇒ nAl=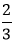 nS=
nS=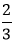 .0,1=
.0,1=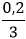 mol
mol
Vậy mAl=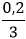 .27=1,8 gam.
.27=1,8 gam.
Ví dụ 3:Muối Al2S3 tạo thành từ phản ứng 2Al + 3S 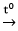 Al2S3 có màu gì?
Al2S3 có màu gì?
A. Màu đen.
B. Màu trắng.
C. Màu đỏ.
D. Màu vàng.
Hướng dẫn giải
Chọn B.
Xem thêm các phương trình hóa học hay khác:


Nội dung được phát triển bởi đội ngũ Meraki Center với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@merakicenter.edu.vn