Nội dung bài viết
Carbon là một nguyên tố hóa học giống như hydro, oxy, chì hoặc bất kỳ nguyên tố nào khác trong bảng tuần hoàn. Nó có ý nghĩa quan trọng nhất của cuộc sống. Không có điều này, sự tồn tại của sự sống là không thể. Bạn có thể nhận thấy rằng carbon là nguyên tố chính trong hầu hết các hợp chất cần thiết cho sự sống. Vậy Cacbon là gì? Tính chất hóa lý của cacbon? Ứng dụng? Để tìm hiểu về vấn đề này chúng ta cùng đọc bài viết dưới đây:
1. Cacbon là gì?
Carbon (ký hiệu hóa học C), là nguyên tố hóa học phi kim loại nằm trong IVa của bảng tuần hoàn. Nó chứa 6 proton trong hạt nhân và do đó có số nguyên tử là 6.
Mặc dù phân bố rộng rãi trong tự nhiên, carbon không nhiều ở khoảng 0,025% vỏ Trái đất nhưng nó tạo thành nhiều hợp chất hơn tất cả các nguyên tố khác cộng lại.
Năm 1961, đồng vị cacbon-12 được chọn để thay thế oxy làm tiêu chuẩn so với trọng lượng nguyên tử của tất cả các nguyên tố khác.
Carbon là nguyên tố thứ 6 trong bảng tuần hoàn
2. Một số tính chất đặc trưng của Carbon
Một số tính chất của cacbon được đưa ra dưới đây:
- Carbon có 4 electron để tạo thành liên kết cộng hóa trị.
- Nó có một số đồng vị và các dạng tồn tại khác như kim cương và than chì với các tính chất đặc biệt.
- Cacbon là một phi kim hóa trị bốn.
- Nguyên tố hóa học này có khả năng liên kết với nhiều nguyên tố.
- Khối lượng nguyên tử: Khối lượng nguyên tử của nó là 12,011 g/mol.
- Độ âm điện: Theo Pauling, độ âm điện của carbon là 2,5.
- Điểm sôi: Điểm sôi của nó là 4827 đọcC.
- Điểm nóng chảy: Điểm nóng chảy của nó là 3652 độ C.
- Mật độ: Mật độ của nó là 2,2 g/cm^3 ở 20 độ C.
- Đồng vị: Nó có ba đồng vị: C-12, C-13, C-14
3. Tính chất hóa lý của Carbon
Tính chất của cacbon như sau:
3.1. Tính chất vật lý của cacbon
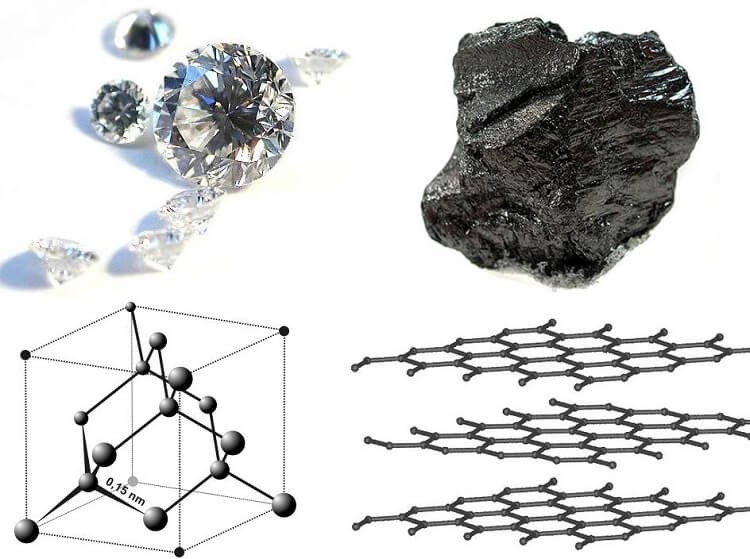
Carbon tồn tại ở nhiều dạng khác nhau như than chì (mềm và xám hoặc đen xỉn), hay kim cương (màu trắng sáng), than củi, than cốc… Trong số đó, một trong những hợp chất quan trọng nhất của carbon là than củi, được hình thành khi đốt nóng carbon. trong trường hợp không có không khí.
Mật độ của các dạng carbon khác nhau phụ thuộc vào nguồn gốc của các nguyên tố này. Có một số dạng carbon tinh khiết và một số dạng không tinh khiết như than đá là hỗn hợp của cả carbon và hydro. Các loại than này thường có cấu trúc xốp và có khả năng hấp thụ các khí mạnh và các chất hòa tan trong dung dịch.
3.2. Tính chất hóa học của cacbon
Đúng là cacbon có mặt trong hầu hết mọi hợp chất nhưng phản ứng hóa học rất yếu so với các nguyên tố khác. Việc so sánh được thực hiện trong điều kiện bình thường. Nếu xét ở áp suất và nhiệt độ tiêu chuẩn, carbon có khả năng chống oxy hóa. Do đó, nó sẽ không phản ứng với axit sulfuric, clo, axit clohydric và các kim loại kiềm khác.
Tuy nhiên, khi nhiệt độ tăng, carbon sẽ phản ứng với oxy và kim loại để tạo thành carbon dioxide và cacbua kim loại tương ứng.
Các hợp chất cacbon thường thể hiện các phản ứng sau:
– Phản ứng đốt cháy:
Như chúng ta biết rằng carbon ở mọi dạng đều cần oxy, nhiệt, ánh sáng và tạo thành carbon dioxide. Khi đốt trong không khí tạo ra khí cacbonic thì gọi là quá trình đốt cháy.
C + O2 -> CO2
– Tác dụng với oxit kim loại: Hỗn hợp màu đen ban đầu chuyển dần sang màu đỏ và làm đục nước vôi trong.
CuO + CO2 -> 2Cu + CO2
Cấu trúc của cacbon
4. Ứng dụng của Carbon
Nó là một nguyên tố phi kim loại có nhiều ứng dụng khác nhau. Việc sử dụng carbon và các hợp chất của nó như sau:
– Các mảnh kim cương hoặc bột đen trong vành xe ô tô hay mực máy in, tản nhiệt trong các thiết bị điện tử… Kim cương đặc biệt được sử dụng để làm đồ trang sức quý hiếm.
– Than chì là một dạng cacbon khác được sử dụng làm nồi nấu kim loại ở nhiệt độ cao, điện cực đèn hồ quang, pin khô hoặc làm đầu bút chì, vật liệu chịu lửa, chất bôi trơn. ..
– Còn một dạng cacbon vô định hình khác được sử dụng ở dạng chất tẩy trắng và chất hấp thụ khí, than hoạt tính trong mặt nạ phòng độc…
– Than đá, than củi… được dùng làm nhiên liệu trong công nghiệp hoặc để điều chế một số kim loại…
– Carbon-14, có tính phóng xạ, là đồng vị được sử dụng trong xác định niên đại bằng carbon phóng xạ và đánh dấu phóng xạ.
Hợp chất cacbon có nhiều công dụng như:
+ Sử dụng CO2 và bình chữa cháy.
+ Đá khô là dạng rắn của cacbon.
+ Carbon monoxide có tác dụng khử trong một số quá trình luyện kim.
+ Sản xuất dung môi công nghiệp, carbon disulphide và carbon tetrachloride là một số nguyên liệu đáng chú ý.
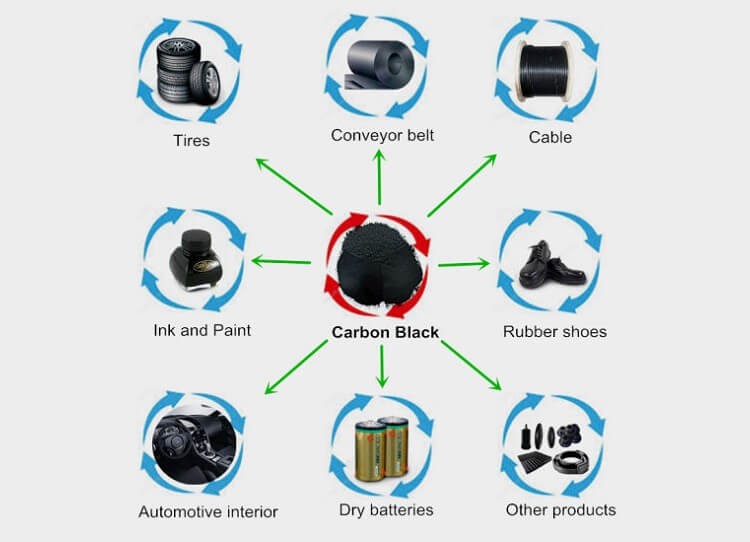
Một số ứng dụng của cacbon
Trên đây là thông tin về carbon. Nếu có thắc mắc, bạn có thể liên hệ với chúng tôi qua đường dây nóng hoặc đọc các bài viết khác trên website Meraki Center của chúng tôi.


Nội dung được phát triển bởi đội ngũ Meraki Center với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: [email protected]