BaCl2 + H2SO4 → BaSO4 + HCl – Hướng dẫn cân bằng phản ứng hóa học của tất cả phương trình hóa học thường gặp giúp bạn học tốt môn Hóa.-BaCl2 + H2SO4 → BaSO4 + HCl
BaCl2 + H2SO4 → BaSO4 + HCl
Phản ứng BaCl2 + H2SO4 tạo ra BaSO4 kết tủa thuộc loại phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất.
Bên cạnh đó là một số bài tập có liên quan về BaCl2 có lời giải, mời các bạn đón xem:
BaCl2 + H2SO4 → BaSO4 ↓ + 2HCl
1. Phương trình phản ứng BaCl2 tác dụng với H2SO4
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Phản ứng này thuộc loại phản ứng trao đổi.
2. Cách tiến hành phản ứng BaCl2 tác dụng với H2SO4
– Nhỏ từ từ từng giọt H2SO4 vào ống nghiệm có chứa sẵn BaCl2.
3. Hiện tượng của phản ứng BaCl2 tác dụng với H2SO4
– Xuất hiện kết tủa màu trắng của BaSO4.
4. Cách viết phương trình ion thu gọn của phản ứng BaCl2 tác dụng với H2SO4
Bước 1: Viết phương trình phân tử:
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Bước 2: Viết phương trình ion đầy đủ bằng cách: chuyển các chất vừa dễ tan, vừa điện li mạnh thành ion; các chất điện li yếu, chất kết tủa, chất khí để nguyên dưới dạng phân tử:
Ba2+ + 2Cl– + 2H+ + SO42- → BaSO4 + 2H+ + 2Cl–
Bước 3: Viết phương trình ion thu gọn từ phương trình ion đầy đủ bằng cách lược bỏ đi các ion giống nhau ở cả hai vế:
Ba2+ + SO42- → BaSO4↓
5. Mở rộng về phản ứng trao đổi trong dung dịch chất điện li
Xét phản ứng:
Dung dịch A + dung dịch B → Sản phẩm.
– Phản ứng xảy ra trong dung dịch các chất điện li là phản ứng giữa các ion.
– Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất 1 trong số các chất sau:
+ Chất kết tủa.
+ Chất điện li yếu.
+ Chất khí.
Thí dụ:
+ Phản ứng tạo thành chất kết tủa:
Na2SO4 + BaCl2 → 2NaCl + BaSO4↓
+ Phản ứng tạo thành chất điện li yếu:
HCl + NaOH → NaCl + H2O
+ Phản ứng tạo thành chất khí:
Fe + H2SO4 loãng → FeSO4 + H2↑
6. Mở rộng kiến thức về H2SO4
6.1. Tính chất vật lí
– Axit sunfuric (H2SO4) là chất lỏng sánh như dầu, không màu, không bay hơi, nặng gần gấp 2 lần nước (H2SO4 98% có D = 1,84 g/cm3).
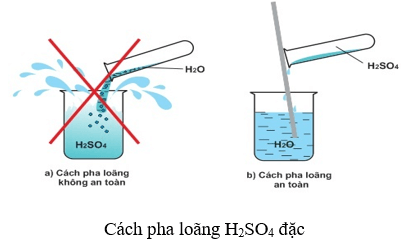
– H2SO4 tan vô hạn trong nước và toả nhiệt rất nhiều nhiệt. Nếu ta rót nước vào H2SO4, nước sôi đột ngột và kéo theo những giọt axit bắn ra xung quanh gây nguy hiểm.
– Cách pha loãng axit sunfuric đặc an toàn: Rót từ từ axit vào nước và khuấy nhẹ bằng đũa thuỷ tinh mà không được làm ngược lại.
6.2. Tính chất hóa học
a. Tính chất của dung dịch axit sunfuric loãng
H2SO4 loãng có đầy đủ tính chất của một axit mạnh.
– Làm đổi màu quỳ tím thành đỏ
– Tác dụng với nhiều kim loại (Mg, Al, Zn, Fe,…) tạo thành muối sunfat và giải phóng khí hiđro.
Ví dụ:
H2SO4 (loãng) + Mg → MgSO4 + H2 (↑)
3H2SO4 (loãng) + 2Al → Al2(SO4)3 + 3H2 (↑)
Chú ý: Các kim loại Hg, Cu, Ag, Au, Pt …không tác dụng với H2SO4 loãng.
Khi Fe tác dụng với H2SO4 loãng, sản phẩm thu được là muối sắt (II)
H2SO4 (loãng) + Fe → FeSO4 + H2 (↑)
– Tác dụng với bazơ tạo thành muối sunfat và nước.
Ví dụ:
H2SO4 + Cu(OH)2 → CuSO4 + 2H2O
H2SO4 + 2KOH → K2SO4 + 2H2O
– Tác dụng với basic oxide tạo thành muối sunfat và nước.
Ví dụ:
H2SO4 + CuO → CuSO4 + H2O
H2SO4 + Na2O → Na2SO4 + H2O
– Tác dụng với một số muối tạo thành muối sunfat và axit mới
Ví dụ:
MgCO3 + H2SO4 → MgSO4 + CO2 ↑ + H2O
b. Tính chất của axit sunfuric đặc
– Tính oxi hóa mạnh
+ Axit sunfuric đặc oxi hoá hầu hết các kim loại (trừ Au và Pt) tạo muối hoá trị cao và thường giải phóng SO2 (có thể H2S, S nếu kim loại khử mạnh như Mg).
2Fe + 6H2SO4 →to Fe2(SO4)3 + 3SO2 + 6H2O
Cu + 2H2SO4 →to CuSO4 + SO2 + 2H2O
Chú ý: Al, Fe, Cr bị thụ động hóa trong H2SO4 đặc, nguội.
+ Tác dụng với nhiều phi kim:
C + 2H2SO4 →to CO2 + 2SO2 + 2H2O
S + 2H2SO4 →to 3SO2 + 2H2O
+ Tác dụng với nhiều hợp chất có tính khử:
2FeO + 4H2SO4 →to Fe2(SO4)3 + SO2 + 4H2O
2KBr + 2H2SO4 →to Br2 + SO2 + 2H2O + K2SO4
Ngoài ra H2SO4 đặc có tính háo nước:
Axit sunfuric đặc chiếm nước kết tinh của nhiều muối ngậm nước, hoặc chiếm các nguyên tố H và O (thành phần của nước) trong nhiều hợp chất.
Ví dụ:
Khi cho axit H2SO4 đặc vào đường, đường sẽ hóa thành than.
C12H22O11 →H2SO4 đ12C + 11H2O
Sau đó một phần C sinh ra lại bị H2SO4 đặc oxi hóa:
C + 2H2SO4 (đặc) → CO2 + 2SO2 + 2H2O
6.3. Ứng dụng
– Axit sunfuric là hoá chất hàng đầu được dùng trong nhiều ngành sản xuất. Hàng năm, các nước trên thế giới sản xuất khoảng 160 triệu tấn H2SO4.
– Axit sunfuric được dùng để sản xuất phân bón, thuốc trừ sâu, chất giặt rửa tổng hợp, tơ sợi hoá học, chất dẻo, sơn màu, phẩm nhuộm, dược phẩm, chế biến dầu mỏ…
6.4. Sản xuất
Axit sunfuric được sản xuất trong công nghiệp bằng phương pháp tiếp xúc. Phương pháp này có 3 công đoạn chính:
– Sản xuất sulfur dioxide (SO2)
Phụ thuộc vào nguồn nguyên liệu có sẵn, người ta đi từ nguyên liệu ban đầu là lưu huỳnh hoặc pirit sắt FeS2…
+ Đốt cháy lưu huỳnh: S + O2 →to SO2
+ Đốt quặng pirit sắt FeS2:4FeS2 + 11O2 →to 2Fe2O3 + 8SO2
– Sản xuất sulfur trioxide (SO3)
Oxi hoá SO2 bằng khí oxi hoặc không khí dư ở nhiệt độ 450 – 5000C, xúc tác V2O5:
2SO2 + O2 ⇄to,xt2SO3
– Hấp thụ SO3 bằng H2SO4
Dùng H2SO4 98% hấp thụ SO3, được oleum H2SO4 .nSO3:
H2SO4 + nSO3 → H2SO4 .nSO3
Sau đó dùng lượng nước thích hợp pha loãng oleum, được H2SO4 đặc:
H2SO4 .nSO3 + nH2O → (n + 1) H2SO4
7. Bài tập vận dụng liên quan
Câu 1: Hòa tan hoàn toàn Fe3O4 trong dung dịch H2SO4 loãng (dư) được dung dịch X1. Cho lượng dư bột Fe vào dung dịch X1 (trong điều kiện không có không khí) đến khi phản ứng xảy ra hoàn toàn, thu được dung dịch X2 chứa chất tan
A.FeSO4.
B.FeSO4 và H2SO4
C.Fe2(SO4)3 và H2SO4.
D.Fe2(SO4)3.
Hướng dẫn giải:
Đáp án A
Fe3O4 + 4H2SO4 loãng,dư→ FeSO4 + Fe2(SO4)3 + 4H2O
Vì H2SO4 dư nên dung dịch X1 gồm (FeSO4 , Fe2(SO4)3 và H2SO4 dư)
Cho Fe dư vào dd X1: Fe2(SO4)3 + Fedư → 3FeSO4
H2SO4dư + Fedư → FeSO4 + H2
Vì Fe dư nên Fe2(SO4)3 và H2SO4 dư đều hết → dd X2 chỉ có FeSO4
(có thể làm nhanh, Fe dư sau phản ứng thì toàn bộ lượng Fe3+ chuyển thành Fe2+, nên khi đề cho Fe dư sau phản ứng chỉ thu được muối Fe2+
Câu 2: Dãy kim loại phản ứng được với dung dịch H2SO4 loãng là:
A. Ag, Ba, Fe, Sn
B. Cu, Zn, Na, Ba
C. Au, Pt
D. K, Mg, Al, Fe, Zn
Hướng dẫn giải:
Đáp án D
Những kim loại đứng trước H trong dãy hoạt động hóa học của kim loại thì phản ứng được với axit H2SO4 loãng, HCl…
Dãy hoạt động hóa học của một số kim loại:
K, Na, Ba, Ca, Mg, Al, Zn, Fe, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, Au
Câu 3: Cho 0,52 gam hỗn hợp 2 kim loại Mg, Al tan hoàn toàn trong dung dịch H2SO4 loãng dư thu được 0,336 lít khí ở đktc. Khối lượng muối sunfat thu được là:
A. 1,24gam
B. 6,28gam
C. 1,96gam
D. 3,4gam.
Hướng dẫn giải:
Đáp án C
Áp dụng nhanh công thức:
mmuối = mKL + mSO42− = 0,52 + 0,015. 96 = 1,96 gam
Câu 4:Cho 21 gam hỗn hợp Zn và CuO phản ứng vừa đủ với 600 ml dung dịch H2SO4 0,5M. Phần trăm khối lượng của Zn có trong hỗn hợp ban đầu là
A. 57%
B. 62%
C. 69%
D. 73%
Hướng dẫn giải:
Đáp án B
Đặt nZnSO4=x molnCuSO4=y mol
→ 65x + 80y = 21 (1)
nSO42−=nH2SO4→x + y = 0,3 mol (2)
→ x = 0,2 mol; y = 0,1 mol
→ %mZn= 62%
Câu 5:Hòa tan 0,4 gam SO3 vào a gam dung dịch H2SO4 10% thu được dung dịch H2SO4 12,25%. Giá trị của a là
A. 20,6 gam
B. 16,9 gam
C. 26,0 gam
D. 19,6 gam
Hướng dẫn giải:
Đáp án D
Khi hòa tan SO3 vào dung dịch xảy ra phản ứng:
SO3 + H2O → H2SO4
Khối lượng của H2SO4:
mH2SO4=0,4.9880+a.10100=0,1a+0,49(g)
Khối lượng dung dịch: m dd = a + 0,4 (g)
Ta có:
C%=0,1a+0,49a+0,4.100%=12,25%→a=19,6(g)
Câu 6:Cho m gam hỗn hợp 2 kim loại Mg, Al tan hoàn toàn trong dung dịch H2SO4 loãng dư thu được 0,336 lít khí ở đktc. Dung dịch thu được sau phản ứng chứa 1,96 gam muối tan. Giá trị của m là
A. 0,24 gam
B. 0,28 gam
C. 0,52 gam
D. 0,4 gam.
Hướng dẫn giải:
Đáp án C
Áp dụng nhanh công thức :
nSO42−môi trường = 0,5.n e nhận = nSO2 = 0,015 mol
mmuối = mKL + mSO42−
⇒ mKL = 1,96 – 0,015.96 = 0,52 gam.
Câu 7: Cho 2,81 gam hỗn hợp gồm 3 oxit Fe2O3, MgO, ZnO tan vừa đủ trong 300ml dung dịch H2SO4 0,1M thì khối lượng muối sunfat khan tạo thành là:
A. 5,33gam
B. 5,21gam
C. 3,52gam
D. 5,68gam.
Hướng dẫn giải:
Đáp án B
nO (oxit) = nH+2= 0,03 mol
→ mKL = m oxit – mO(oxit) = 2,81 – 0,03.16 = 2,33 gam
mmuối = mKL + mSO42− = 2,33 + 0,03.96 = 5,21gam
Câu 8:Cho 20g hỗn hợp X gồm Fe, Cu phản ứng hoàn toàn với H2SO4 loãng dư, sau phản ứng thu được 12g chất rắn không tan. Phần trăm về khối lượng của Fe trong X:
A. 60%
B. 72%
C. 40%
D. 64%
Hướng dẫn giải:
Đáp án C
Cu không tác dụng với H2SO4 loãng, nên chất rắn không tan là Cu
→ mCu = 12g → mFe = 20-12 = 8g
→ %mFe = 40%
Câu 9:Cho 15,82 gam hỗn hợp Al, Fe, Cu tác dụng hết với dung dịch H2SO4 đặc nóng thu được dung dịch A và 9,632 lít khí SO2 ở đktc. Cô cạn dung dịch A sẽ thu được số gam muối khan là:
A. 57,1gam
B. 60,3 gam
C. 58,8 gam
D. 54,3 gam
Hướng dẫn giải:
Đáp án A
nSO42−môi trường = nSO2= 0,43mol
→ mmuối = mKL + mSO42−= 15,82 + 0,43. 96 = 57,1 gam
Câu 10: Cho 18 gam kim loại M tác dụng với dung dịch H2SO4 đặc nóng dư thu được 3,36 lít khí SO2 ở đktc và 6,4 gam S và dung dịch X. Cô cạn dung dịch X thu được số gam muối khan là:
A. 75 gam
B. 90 gam
C. 96 gam
D. 86,4 gam
Hướng dẫn giải:
Đáp án B
nSO42−tạo muối = 0,5.n e nhận= nSO2+ 3nS
= 0,15 + 3.0,2= 0,75mol
mmuối = mKL + mSO42−= 18 + 0,75. 96= 90 gam
Câu 11: Cho 6,72 gam Fe vào dung dịch chứa 0,3 mol H2SO4 đặc, nóng (giả thiết SO2 là sản phẩm khử duy nhất). Sau khi phản ứng xảy ra hoàn toàn, thu được
A.0,03mol Fe2(SO4)3và 0,06 mol FeSO4
B.0,05mol Fe2(SO4)3và 0,02 mol Fe dư
C.0,02mol Fe2(SO4)3và 0,08 mol FeSO4
D.0,12mol FeSO4.
Hướng dẫn giải:
Đáp án A
nFe = 0, 12 mol
2Fe + 6H2SO4→ Fe2(SO4) 3+ 3SO2 +6H2O
0,1 ←0,3→ 0,05mol
Fedư + Fe2(SO4)3 → 3FeSO4
(0,12-0,1) → 0,02 0,06
nFeSO4=0,06 mol;nFe2(SO4)3 du=0,05−0,02=0,03 mol
Câu 12: Dùng 300 tấn quặng pirit (FeS2) có lẫn 20% tạp chất để sản xuất axit H2SO4 có nồng độ 98%. Biết rằng hiệu suất phản ứng là 90%. Khối lượng axit H2SO4 98% thu được là
A. 320 tấn
B. 335 tấn
C. 350 tấn
D. 360 tấn
Hướng dẫn giải:
Đáp án D
Ta có sơ đồ :
FeS2 →2SO2 →2SO3 →2H2SO4
120→ 2.98gam
300.0,8 → x tấn
→ Theo lý thuyết thì: mH2SO4=0,8.300.2.98120=392tấn
Thực tế thì mdd H2SO4 98%=392.0,9.10098=360tấn
Câu 13:Cho x mol Fe tan hoàn toàn trong dung dịch chứa y mol H2SO4 (tỉ lệ x : y = 2 : 5) thu được một sản phẩm khử duy nhất là SO2 và dung dịch chỉ chứa muối sunfat. Số mol electron do lượng Fe trên nhường khi bị hòa tan là
A. 2x.
B. 3x.
C. 2y.
D.y.
Hướng dẫn giải:
Đáp án D
Gọi số mol Fe nhường là a
Ta có: nSO42−= 0,5 n e nhường = 0,5a
nSO2= 0,5n e nhận = 0,5a
Bảo toàn nguyên tố S: nH2SO4=nSO42−+nSO2=a=y
Xem thêm các phương trình hóa học hay khác:


Nội dung được phát triển bởi đội ngũ Meraki Center với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@merakicenter.edu.vn