C2H2 + H2O → CH3CHO | acetylene + nước | C2H2 ra CH3CHO – Hướng dẫn cân bằng phản ứng hóa học của tất cả phương trình hóa học thường gặp giúp bạn học tốt môn Hóa.-C2H2 + H2O → CH3CHO | acetylene + nước | C2H2 ra CH3CHO
C2H2 + H2O → CH3CHO | acetylene + nước | C2H2 ra CH3CHO
Phản ứng acetylene + nước hay C2H2 + H2O tạo ra CH3CHO thuộc loại phản ứng cộng đã được cân bằng chính xác và chi tiết nhất.
Bên cạnh đó là một số bài tập có liên quan về C2H2 có lời giải, mời các bạn đón xem:
C2H2 + H2O → CH3CHO
1. Phương trình phản ứng acetylene tác dụng với nước
CH ≡ CH + H2O →HgSO4, H2SO4 CH3 – CH = O
2. Điều kiện của phản ứng acetylene tác dụng với nước
– Xúc tác: HgSO4, H2SO4
3. Cách tiến hành phản ứng acetylene tác dụng với nước
– Sục khí acetylene vào nước đun nóng có xúc tác HgSO4 trong môi trường axit.
4. Mở rộng về tính chất hoá học của alkyne
4.1. Phản ứng cộng
a) Cộng hiđro
– Khi có niken (hoặc platin hoặc palađi) làm xúc tác, alkyne cộng hiđro tạo thành alkene, sau đó tạo thành alkane.
Thí dụ:
CH ≡ CH + H2 →Ni, to CH2 = CH2
CH2 = CH2 + H2 →Ni, to CH3 – CH3
– Lưu ý: Khi dùng xúc tác là hỗn hợp Pd/PbCO3 hoặc Pd/BaSO4, alkyne chỉ cộng một phân tử hiđro tạo thành alkene.
CH ≡ CH + H2 →Pd/PbCO3, to CH2 = CH2
⇒ Đặc tính này được dùng để điều chế alkene từ alkyne.
b) Cộng brom, clo
– Brom và clo cũng tác dụng với alkyne theo hai giai đoạn liên tiếp.
Thí dụ:
CH ≡ CH + Br2 → CHBr = CHBr
CHBr = CHBr + Br2 → CHBr2 – CHBr2
c) Cộng HX (X là OH, Cl, Br, CH3COO…)
– alkyne tác dụng với HX theo hai giai đoạn liên tiếp.
Thí dụ:
CH ≡ CH + HCl →to, xt CH2 = CHCl
CH2 = CHCl + HCl →to, xt CH3 – CHCl2
– Khi có xúc tác thích hợp, alkyne tác dụng với HCl sinh ra dẫn xuất monochloro của alkene.
Thí dụ:
CH ≡ CH + HCl →150−200CoHgCl2 CH2 = CHCl
– Phản ứng cộng HX của các alkyne cũng tuân theo quy tắc Mac-côp-nhi-côp.
– Phản ứng cộng H2O của các alkyne chỉ xảy ra theo tỉ lệ số mol 1:1.
Thí dụ:
CH ≡ CH + H2O →HgSO4, H2SO4 CH3 – CH = O (anehit axetic)
d) Phản ứng đime và trime hoá
2CH ≡ CH →to, xt CH ≡ C – CH = CH2 (vinylacetylene)
3CH ≡ CH →bôt C600Co C6H6 (benzen)
4.2. Phản ứng thế bằng ion kim loại
– Sục khí acetylene vào dung dịch silver nitrate trong amonia, thấy có kết tủa vàng nhạt.
CH ≡ CH + 2AgNO3 + 2NH3 → Ag – C ≡ C – Ag↓ + 2NH4NO3

Phản ứng thế nguyên tử hidro của C2H2 bằng ion bạc
a) Trước khi sục khí C2H2.
b) Sau khi sục khí C2H2.
Kết luận:
– Nguyên tử hiđro liên kết trực tiếp với nguyên tử cacbon liên kết ba đầu mạch có tính linh động cao hơn các nguyên tử hiđro khác nên có thể bị thay thế bằng ion kim loại.
– Các ank-1-yne khác như propin, but-1-in, … cũng có phản ứng tương tự acetylene.
⇒ Tính chất này được dùng để phân biệt ank-1-yne với alkene và các alkyne khác.
4.3. Phản ứng oxi hoá
a) Phản ứng oxi hoá hoàn toàn (cháy)
Các alkyne cháy toả nhiều nhiệt:
2CnH2n – 2 + (3n – 1)O2 →to 2nCO2 + 2(n – 1)H2O
b) Phản ứng oxi hoá không hoàn toàn
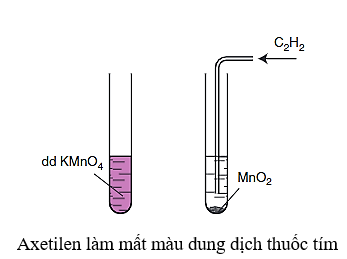
– Tương tự alkene và alkadien, alkyne cũng có khả năng làm mất màu dung dịch thuốc tím.
5. Bài tập vận dụng liên quan
Câu 1: Có bao nhiêu alkyne ứng với công thức phân tử C5H8 ?
A. 2.
B. 4
C. 3.
D. 1.
Hướng dẫn giải:
Đáp án C
Có 3 công thức thỏa mãn :
CH≡C – CH2 – CH2 – CH3
CH3 – C≡C – CH2 – CH3
CH≡C – CH(CH3) – CH3
Câu 2: X là hydrocarbon mạch hở, phân nhánh, có công thức phân tử C5H8. Biết X có khả năng làm mất màu nước brom và tham gia phản ứng với AgNO3 trong dung dịch NH3. Tên của X theo IUPAC là :
A. 2-methylbut-3-in
B. 3-methylbut-1-yne
C. 2-methylButa -1,3- diene
D. pent-1-in
Hướng dẫn giải:
Đáp án B
X phản ứng với AgNO3/NH3 → có nối 3 đầu mạch
→ X là CH≡C-CH(CH3)2 (3-methylbut-1-in)
Câu 3:Hidrat hóa có xúc tác 3,36 lit C2H2(dktc) thu được hỗn hợp A (hiệu suất phản ứng 60%). Cho hỗn hợp A tác dụng với AgNO3/NH3 thu được m gam kết tủa. Giá trị của m là :
A. 48,24
B.33,84
C.14,4
D.19,44
Hướng dẫn giải:
Đáp án B
nC2H2=0,15 mol
C2H2 + H2O →to,xt CH3CHO
→nCH3CHO=0,15.60100=0,09 mol→nC2H2(du)=0,15−0,09=0,06 mol
C2H2 →AgNO3/NH3 Ag2C2 ↓
CH3CHO →AgNO3/NH3 2Ag ↓
Câu 4:Dẫn hỗn hợp khí X gồm etilen và acetylene qua bình đựng dung dịch AgNO3 trong NH3 (dư) đến khi phản ứng xảy ra hoàn toàn thì thu được 28,8 gam kết tủa và thấy có 2,912 lít khí (đo ở đktc) thoát ra. Phần trăm khối lượng của acetylene trong X là
A. 53,85%.
B. 46,15%.
C. 50,15%.
D. 49,85%.
Hướng dẫn giải:
Đáp án B
Chỉ có C2H2 phản ứng tạo Ag2C2
→nC2H4=2,91222,4=0,13 mol
nC2H2=nAg2C2=28,8240=0,12 mol
→%mC2H2=0,12.260,12.26+0,13.28.100%=46,15%
Câu 5:Hỗn hợp X gồm 2 alkyne. Đốt cháy hoàn toàn 0,05 mol hỗn hợp X trên thu được 0,17 mol CO2. Mặt khác cứ 0,05 mol hỗn hợp X phản ứng vừa đủ với 300 ml dung dịch AgNO3 0,1M trong dung dịch NH3. Hỗn hợp X là :
A. acetylene, but – 1 – in
B. acetylene, propin
C. propin, but – 1 – in
D. propin, but – 2 – in
Hướng dẫn giải:
Đáp án D
Số C trung bình 2 alkyne = 0,170,05=3,4
Vì nAgNO3<nX→ Trong X có 1 alkyne không phản ứng với AgNO3
Dựa vào đáp án → Chỉ có đáp án D thỏa mãn vì but – 2 – in không phản ứng với AgNO3
Câu 6: Trong phân tử alkyne X, hidro chiếm 11,76% khối lượng. Công thức phân tử của X là :
A. C2H2
B. C5H8
C. C4H6
D. C3H4
Hướng dẫn giải:
Đáp án B
Công thức alkyne là CnH2n-2 (n ≥ 2)
→%mH=2n−214n−2.100%=11,76%
→ n = 5
Vậy X là C5H8
Câu 7: Đốt cháy hoàn toàn 1 lít hỗn hợp khí gồm C2H2 và hydrocarbon X sinh ra 2 lít khí CO2 và 2 lít hơi H2O (các thể tích khí và hơi đo trong cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của X là
A. C2H4.
B. CH4.
C. C2H6.
D. C3H8.
Hướng dẫn giải:
Đáp án C
Ta có: C=nCO2nhh=21=2→ hydrocarbon X cũng có 2C.
H=2nH2Onhh=2.21=4→Hydrocarbon X có số H lớn hơn 4
→ có số H = 6
→ X là C2H6
Câu 8:alkyne C6H10 có bao nhiêu đồng phân phản ứng với dung dịch AgNO3/NH3 ?
A. 3
B. 4
C. 5
D. 6
Hướng dẫn giải:
Đáp án B
CH≡C-CH2-CH2-CH2-CH3
CH≡C-CH2-CH(CH3)-CH3
CH≡C-CH(CH3)-CH2-CH3
CH≡C-C(CH3)3
Vậy có 4 đồng phân thỏa mãn đề bài.
Câu 9:Hỗn hợp khí A gồm 0,6 mol H2 và 0,15 mol vinylacetylene. Nung A một thời gian với xúc tác Ni thu được hỗn hợp B có tỉ khối so với H2 bằng 10. Dẫn hỗn hợp B qua dung dịch brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là:
A. 16.
B. 0.
C. 24.
D. 8.
Hướng dẫn giải:
Đáp án C
BTKL: ns.Ms = nđ.Mđ → 0,6.2 + 0,15.52 = ns.20 → ns = 0,45 mol
Số mol khí sau phản ứng giảm là số mol H2 phản ứng:
nH2= nđ – ns = 0,75 – 0,45 = 0,3 mol
BT liên kết π ta có: n π đầu – n π pư = n π sau hay 3nvinylacetylene – pư = nBr2
→nBr2pư = 3.0,15 – 0,3 = 0,15 mol
→mBr2= 0,15.160 = 24 gam
Câu 10:Hỗn hợp khí X chứa H2 và một alkyne. Tỉ khối của X đối với H2 là 3,4. Đun nóng nhẹ X có mặt xúc tác Ni thì nó biến thành hỗn hợp Y không làm mất màu nước brom và có tỉ khối đối với H2 là 34/6. Công thức phân tử của alkyne là :
A. C2H2
B. C3H4
C. C4H6
D. C4H8
Hướng dẫn
Đáp án A
M¯X=3,4.2=6,8; M¯Y=346.2=343
Chọn số mol hỗn hợp X là 1 mol (nX = 1 mol) → mX = 6,8 (g)
BTKL mX = mY = 6,8 (g) → nY = 6,8343 =0,6 mol
nH2(phan ung)= nX – nY = 1 – 0,6 = 0,4 mol
Vì hỗn hợp Y không làm mất màu nước Br2 nên trong Y chỉ có alkane.
CnH2n-2 + 2H2 →to,xtCnH2n+2 (n≥2)
Theo phương trình mol alkyne = 12 mol H2 phản ứng = 0,2 mol
mX = (14n – 2).0,2 + 2(1 – 0,2) = 6,8 → n = 2. CTPT: C2H2.
Câu 11: Đốt cháy m gam hỗn hợp C2H6, C3H4, C3H8, C4H10 được 35,2 gam CO2 và 21,6 gam H2O. Giá trị của m là
A. 14,4.
B. 10,8.
C. 12.
D. 56,8.
Hướng dẫn giải:
Đáp án C
m hydrocarbon = mC + mH = = 12g
Câu 28: alkyne là những hydrocarbon không no, mạch hở, có công thức chung là
A. CnH2n+2 (n ≥ 1).
B. CnH2n (n ≥ 2).
C. CnH2n-2 (n ≥ 2).
D. CnH2n-6 (n ≥ 6).
Hướng dẫn giải:
Đáp án C
alkyne là những hydrocarbon không no, mạch hở, có công thức chung là CnH2n-2
(n ≥ 2).
Câu 12: Dẫn hỗn hợp X gồm 0,05 mol C2H2, 0,1 mol C3H4 và 0,1 mol H2 qua ống chứa Ni nung nóng một thời gian thu được hỗn hợp Y gồm 7 chất. Đốt cháy hoàn toàn Y bằng O2 dư rồi cho sản phẩm cháy hấp thụ hết vào 700 ml dung dịch NaOH 1M, thu được dung dịch Z. Tổng khối lượng chất tan trong Z là
A. 35,8
B. 45,6
C. 38,2
D. 40,2
Hướng dẫn giải:
Đáp án D
Đốt cháy Y cũng là cháy X
BTNT “C” → nCO2=2nC2H2+3nC3H4=0,4
Lại có: nCO2<nNaOH<2nCO2
→ tạo 2 muối Na2CO3 và NaHCO3
Trong đó nNa2CO3=nOH−−nCO2 = 0,3 mol
→nNaHCO3=0,4−0,3=0,1 mol
m chất tan trong Z = 0,3.106 + 0,1.84 = 40,2g
Xem thêm các phương trình hóa học hay khác:


Nội dung được phát triển bởi đội ngũ Meraki Center với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@merakicenter.edu.vn