C2H2 + O2 → CO2 + H2O | Đốt cháy acetylene – Hướng dẫn cân bằng phản ứng hóa học của tất cả phương trình hóa học thường gặp giúp bạn học tốt môn Hóa.-C2H2 + O2 → CO2 + H2O | Đốt cháy acetylene
C2H2 + O2 → CO2 + H2O | Đốt cháy acetylene
Phản ứng đốt cháy acetylene hay C2H2 + O2 thuộc loại phản ứng oxi hóa hoàn toàn đã được cân bằng chính xác và chi tiết nhất.
Bên cạnh đó là một số bài tập có liên quan về C2H2 có lời giải, mời các bạn đón xem:
2C2H2 + 5O2  4CO2 + 2H2O
4CO2 + 2H2O
Điều kiện phản ứng
– Nhiệt độ cao.
Cách thực hiện phản ứng
– Đốt cháy acetylene trong oxi ở điều kiện nhiệt độ cao.
Hiện tượng nhận biết phản ứng
– Khi đốt cháy acetylene trong oxi ở điều kiện nhiệt độ cao thì thấy có khí không màu thoát ra (CO2).
Bạn có biết
– Phản ứng trên là phản ứng oxi hóa hoàn toàn.
– Phản ứng cháy của acetylene tỏa nhiều nhiệt.
– Số mol CO2 > H2O và số mol alkyne phản ứng bằng hiệu số mol của CO2 và H2O.
Ví dụ 1: Đốt cháy hoàn toàn 5,6 lít hỗn hợp methane và acetylene cần 13,44 lít oxi. Phần trăm thể tích acetylene trong hỗn hợp là?
A. 20%
B. 40%
C. 60%
D. 80%
Hướng dẫn:
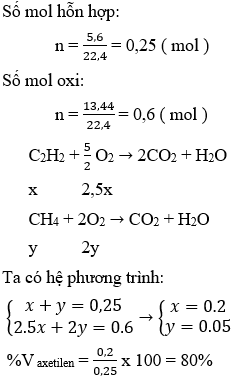
Đáp án D
Ví dụ 2: Đốt cháy hoàn toàn khí acetylene rồi sục hỗn hợp khí thu được qua dung dịch nước vôi trong. Hiện tượng thu được là gì?
A. Kết tủa trắng
B. Có khí thoát ra
C. Không có hiện tượng
D. Dung dịch nước vôi có màu vàng
Hướng dẫn:
2C2H2 + 5O2 → 4CO2 + 2H2O
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Đáp án A
Ví dụ 3: Ứng dụng trong phản ứng cháy của acetylene dùng để làm gì?
A. Làm nguyên liệu sản xuất trong công nghiệp
B. Làm dung môi
C. Hàn cắt kim loại
D. Không có ứng dụng
Hướng dẫn: Vì phản ứng cháy của acetylene tỏa nhiều nhiệt nên được sử dụng trong các đèn xì để hàn cắt kim loại.
Đáp án C.
Xem thêm các phương trình hóa học hay khác:


Nội dung được phát triển bởi đội ngũ Meraki Center với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@merakicenter.edu.vn