Nội dung bài viết
Cation là một ion tích cực, đóng một vai trò quan trọng trong nhiều lĩnh vực khoa học và cuộc sống. Từ hóa học, sinh học đến công nghiệp, cation có nhiều ứng dụng thực tế như trong sản xuất pin, xử lý nước và y học. Vậy cation là gì, loại gì và cách chúng hoạt động? Hãy khám phá chi tiết trong bài viết này.
1. Cation là gì?
Cation là một ion điện tích dương, được hình thành khi một nguyên tử hoặc phân tử mất một hoặc nhiều electron. Do mất các electron, số lượng proton ở người nguyên tử nhiều hơn số lượng electron, làm cho các ion mang điện tích dương.
Ví dụ, một số cation phổ biến:
- Na⁺ (ion natri): xuất hiện trong muối ăn và đóng một vai trò quan trọng trong cân bằng nước của cơ thể.
- K⁺ (ion kali): Cần thiết trong hoạt động của các tế bào thần kinh và cơ bắp.
- Ca²⁺ (ion canxi): Quan trọng trong cấu trúc xương và hoạt động của enzyme.
- Fe²⁺ / Fe³⁺ (ion sắt): Tham gia vào quá trình vận chuyển oxy trong máu.
2. Tính chất của cation
Cation có một số đặc điểm chung giúp phân biệt chúng với anion (các ion tích điện âm):
- Điện tích dương: Do mất các electron, cation có điện tích dương và có xu hướng hấp thụ các ion âm để tạo thành một hợp chất trung hòa.
- Kích thước nhỏ hơn nguyên tử trung tính: khi electron mất, vỏ điện tử của nguyên tử bị thu hẹp, làm giảm kích thước so với trạng thái trung tính.
- Tương tác với anion để tạo ra muối: cation thường được kết hợp với anion để tạo thành một hợp chất ion như NaCl (muối ăn) hoặc caco₃ (đá vôi).
3. Phân loại cation
Cation có thể được phân loại dựa trên điện tích và nguồn gốc:
Phân loại điện
Cation hóa trị (+1): Na⁺, K⁺, Ag⁺ …
Cation multi -chemhother liệu pháp (+2, +3 …): Ca²⁺, Fe²⁺, Fe³⁺, Cu²⁺ …
Phân loại theo sự hình thành phần tử
Cation kim loại: Na⁺, Mg²⁺, Fe³⁺ …
Cation phi kim: H⁺ (ion hydro)
Cation hữu cơ: NH₄⁺ (ammonium), C₆H₅NH₃⁺ (phenylamoni)
Phân loại theo vai trò sinh học
Cation thiết yếu: K⁺, Na⁺, Ca²⁺ có mặt trong cơ thể sống.
Cation độc hại: Pb²⁺ (chì), hg²⁺ (thủy ngân) có thể gây ô nhiễm và ảnh hưởng xấu đến sức khỏe.
4. Áp dụng cation trong cuộc sống
Cation không chỉ đóng một vai trò quan trọng trong hóa học mà còn được sử dụng rộng rãi trong nhiều ngành công nghiệp và sinh học.
Trong ngành công nghiệp
-
Sản xuất pin: Các ion như Li⁺ được sử dụng trong pin lithium-ion.

-
Xử lý nước: Ca²⁺ và Mg²⁺ là nguyên nhân của nước cứng, cần phải loại bỏ để làm mềm nước.
-
Catalytics: Một số cation kim loại như Fe³⁺, Cu²⁺ chơi một chất xúc tác trong các phản ứng hóa học.
Trong sinh học và y học
-
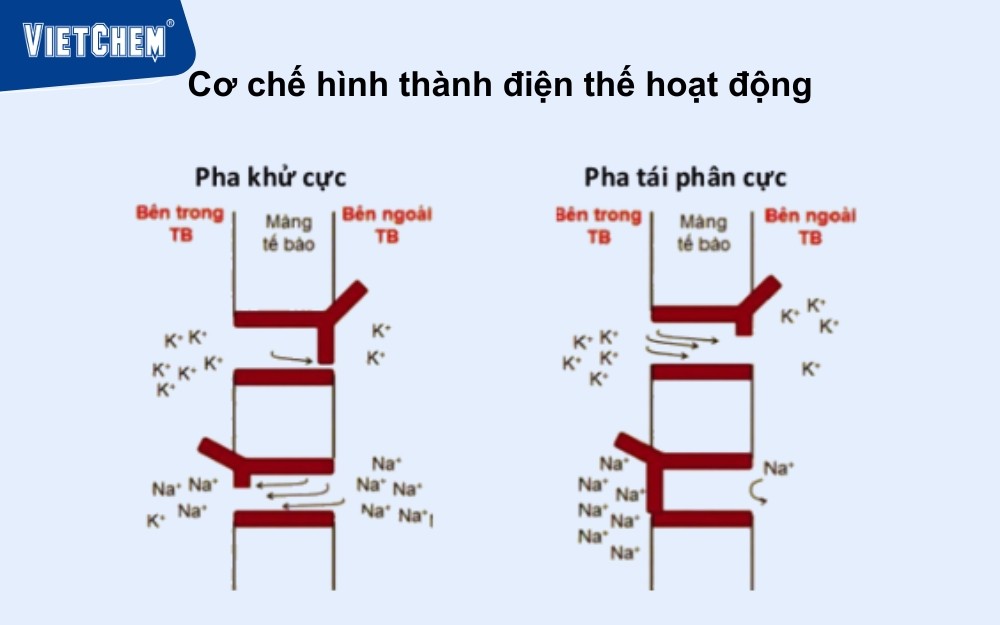
Truyền thần kinh: K⁺ và NA⁺ giúp tạo ra một hoạt động tiềm năng trong các tế bào thần kinh.
-
Cấu trúc xương: Ion canxi (CA²⁺) giúp hình thành và duy trì sức khỏe xương.
-
Vận chuyển oxy: Fe²⁺ trong hemoglobin giúp vận chuyển oxy đến các cơ quan.
Trong nông nghiệp
-
Phân bón: Các cation như K⁺ và NH₄⁺ có mặt trong phân bón để giúp thực vật phát triển.
-
Cân bằng pH đất: Ca²⁺ và Mg²⁺ giúp điều chỉnh độ pH của đất, ảnh hưởng đến sự phát triển của cây.
5. Phân biệt cation và anion
| Tiêu chí | Cation (+) | Anion (-) |
| Định nghĩa | Các ion điện tích dương (mất e) | Các ion có điện tích âm (nhận E) |
| Hình thức | Kim loại mang lại electron để tạo cation | Phi kim nhận electron để tạo anion |
| Ví dụ | Na⁺, K⁺, Ca²⁺, Fe³⁺, Cu²⁺ | Cl⁻, so₄²⁻, no₃⁻, co₃²⁻ |
| Phản ứng công nhận | Phản ứng với dung dịch kiềm (để tạo kết tủa hydroxit, thay đổi màu sắc) | Phản ứng với axit mạnh hoặc các ion kim loại để kết tủa hoặc khí |
| Màu sắc đặc trưng | Một số cation có màu đặc trưng: cu²⁺ (màu xanh), fe³⁺ (màu nâu đỏ) | Anion không màu nhất, ngoại trừ cro₄²⁻ (vàng), mno₄⁻ (màu tím) |
| Đặc tính | Kết tủa hydroxit có thể được tạo ra với NaOH, NH | Có thể kết tủa với Ag⁺, Ba²⁺ hoặc tạo ra khí với H⁺ |
| Nhận dạng ứng dụng | – Sử dụng NaOH, nhưng để tạo kết tủa để xác định các ion kim loại – Sử dụng ngọn lửa (một số cation cho các màu cụ thể: Na⁺ (màu vàng), K⁺ (màu tím), cu²⁺ (màu xanh lá cây)) | – Sử dụng dung dịch Agno₃ (AGCL trắng, Màu vàng sáng AGBR, AGI màu vàng đậm) – Sử dụng bacl₂ để xác định So₄²⁻ (Baso ₄ kết tủa trắng) |

Cation là một thành phần quan trọng trong thế giới hóa học và cuộc sống. Họ không chỉ tham gia vào các phản ứng hóa học mà còn đóng một vai trò thiết yếu trong cơ thể con người, ngành công nghiệp và môi trường. Hiểu cation sẽ giúp chúng ta áp dụng chúng hiệu quả hơn vào khoa học, công nghệ và cuộc sống hàng ngày. Hy vọng rằng bài viết này đã cung cấp cho bạn một cái nhìn tổng quan về cation và các ứng dụng quan trọng của chúng.


Nội dung được phát triển bởi đội ngũ Meraki Center với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@merakicenter.edu.vn